Ormoni maschili: quali sono e come funzionano?

Gli ormoni maschili, anche definiti ormoni androgeni, sono ormoni steroidei che si legano allo specifico recettore degli androgeni che viene attivato e determina una cascata di eventi cellulari.
L’androgeno più famoso è senza dubbio il Testosterone, l’ormone sessuale più abbondante nel maschio, da cui derivano altri due ormoni steroidei molto importanti: il DHT (Diidrotestosterone, androgeno) e il 17-Beta Estradiolo (estrogeno).
Il testosterone ha un ruolo importante come pro-ormone, si ritiene infatti che buona parte dei processi in cui è coinvolto, ad esclusione della sintesi proteica muscolare, siano mediati dal DHT e dall’estradiolo.
Prima di tutto però, vediamo in linea generale come e dove vengono prodotti questi ormoni.
Come e dove vengono prodotti gli ormoni maschili?
Analogamente a molte altre ghiandole endocrine, l’asse endocrino testicolare comprende il sistema ipotalamo-ipofisi.
L’ipotalamo produce fattori peptidici di rilascio, in questo caso si parla di GnRH (da non confondere col GHRH) che stimola la secrezione ipofisaria di gondatropine LH e FSH. L’attività di secrezione del GnRH è regolata dal punto di vista biologico-temporale (si attiva nell’adolescenza), da diversi fattori ormonali (Leptina, Kisspeptina) e non (circuiti neurali).
Le gonadotropine vanno a stimolare direttamente diverse cellule gonadiche, infatti LH agisce sulle cellule di Leydig stimolando la sintesi di steroidi, in particolare il testosterone, mentre FSH (e il Testosterone stesso) stimola nelle cellule del Sertoli la produzione della ABP, una proteina che lega il testosterone, mantenendo quindi alti livelli intratesticolari di testosterone, fondamentale per la fertilità maschile.
Il meccanismo a feedback negativo avviene principalmente ad opera degli steroidi, infatti il testosterone e soprattutto l’estradiolo derivante dall’aromatizzazione del testosterone, sopprimono il rilascio di GnRH e quindi gonadotropine.
Anche altri ormoni intervengono: infatti le cellule del Sertoli secernono inibina B, che agisce inibendo in modo più specifico la secrezione di FSH, inoltre la Prolattina, il Cortisolo, diversi Cannabinoidi gli Oppioidi/Oppiacei inibiscono la secrezione di GnRH.
Il sistema pertanto è strettamente regolato, l’assunzione esogena di steroidi anabolizzanti (AAS) va a perturbare fortemente questo meccanismo, segnalando all’ipotalamo e all’ipofisi la presenza di elevati livelli di steroidi nel sangue (come farebbe il testosterone e l’estradiolo endogeni), con forte o praticamente totale soppressione della secrezione di gonadotropine LH e FSH, inibendo fortemente l’attività del testicolo.
Anche a basse dosi questo avviene, in quanto nella normale fisiologia dell’asse si hanno livelli pulsatili di gonadotropine e quindi della stessa attività testicolare, nel momento in cui le gonadotropine o gli androgeni/estrogeni raggiungono livelli costanti nel tempo, questo asse endocrino viene fortemente disturbato e interrompe la sua attività secretiva.
Questo effetto è infatti sfruttato in medicina nella terapia di privazione androgenica (ADT) per il carcinoma prostatico androgeno dipendente, in pratica si somministra un analogo a lunga azione del GnRH (triptorelina) che causa un iniziale aumento di gonadotropine e testosterone, seguito da una totale soppressione dell’asse.
Testosterone: che cos’è e che funzioni svolge?
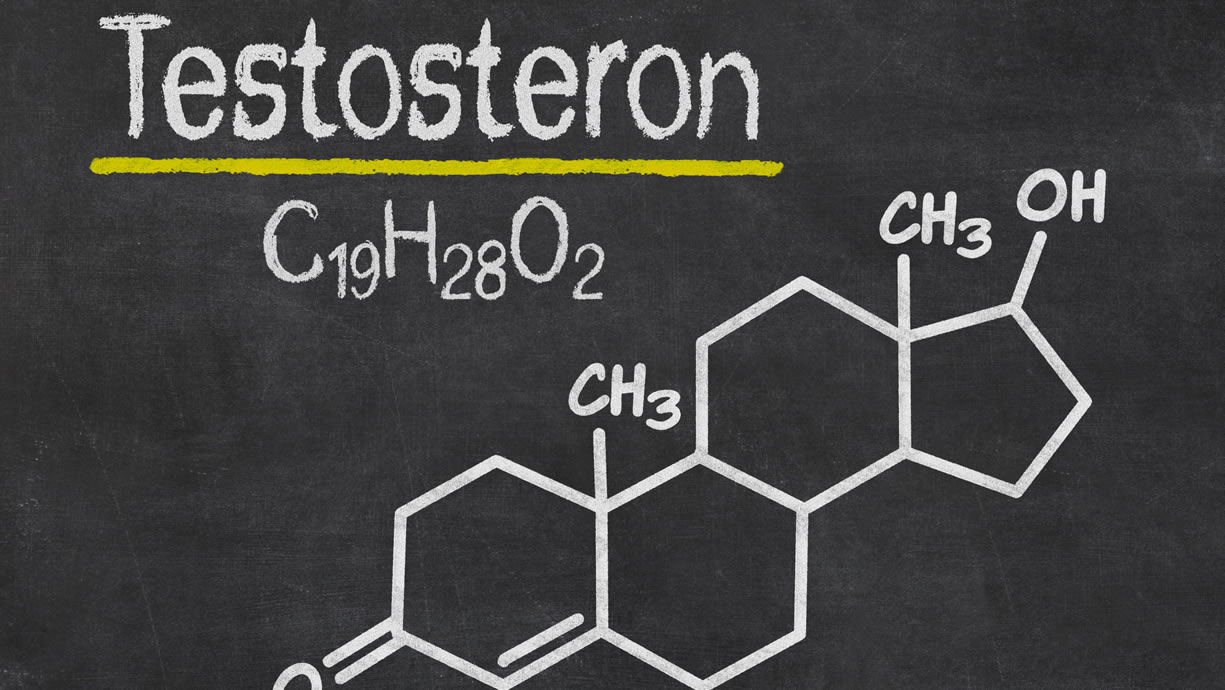
Il testosterone nell’uomo è in gran parte prodotto dalle cellule di Leydig del testicolo, in una quantità di 3-7mg al giorno. Viene prodotto a partire dal colesterolo, che è donato dalle LDL plasmatiche e trasportato attraverso la membrana per subire diversi passaggi enzimatici prima di diventare testosterone.
A proposito di questo aspetto, la broscience vuole che aumentando l’assunzione di colesterolo (con le uova ad esempio) aumenti il testosterone… ecco non accade per diversi motivi:
- il colesterolo plasmatico (nell’adulto sano è in una concentrazione media di 50-129 mg/dl in diversi litri di plasma, fatevi due conti) non è mai un fattore limite, il nostro corpo ne metabolizza diversi grammi al giorno tra sintesi, catabolismo e assorbimento dagli alimenti; il Testosterone è sintetizzato sotto stimolo del LH che non ha alcun legame con l’assunzione alimentare di colesterolo (che per giunta, è metabolizzato dal fegato non dalle gonadi).
- il testosterone, come già accennato, si comporta più da “pro-ormone”, infatti le sue azioni durante lo sviluppo sono mediate in buona parte dal DHT (crescita di peli, allargamento della laringe, libido, temperamento più aggressivo etc…) e dall’estradiolo (ossificazione, libido, crescita tessuti connettivi). Il testosterone è invece responsabile della diversa composizione corporea tra uomo e donna, infatti aumenta la sintesi proteica muscolare, specialmente nei muscoli più ricchi di recettori androgeni (parte alta del tronco) e riduce l’accumulo di tessuto adiposo.
- il testosterone tende fisiologicamente a diminuire con l’età, per insufficienza relative delle cellule di Leydig, ovvero diventano sempre meno responsive alla secrezione di LH ipofisario che non risulta necessariamente ridotto. Questa condizione può portare ad ipogonadismo dell’età adulta (LOH, Late Onest Hypogonadism), che beneficia di terapia sostitutiva con testosterone (TRT).
Tra le varie funzioni del testosterone (e dei metaboliti) nei tessuti, possiamo riassumere le più importanti:
- Muscolo –> aumento della sintesi proteica, ridotto trasporto inverso degli amminoacidi, aumento dell’efficacia di scarica dei motoneuroni, aumento beta-ossidazione e sintesi di glicogeno, reclutamento e mantenimento del pool staminale di cellule satelliti
- Tessuto adiposo–> inibizione della differenziazione delle cellule staminali in adipociti, aumento della lipolisi, riduzione della sintesi di leptina
- Cuore ed endotelio –> mantenimento della funzione cardiovascolare, della sintesi di Ossido Nitrico ma se in eccesso favorisce il suo deterioramento
- Fegato –> aumento del catabolismo e riduzione della sintesi di trigliceridi, se in eccesso aumento della sintesi di LDL e catabolismo HDL
- Reni e Midollo osseo –> stimolo eritropoietico, mantenimento della massa renale, Ritenzione di Sodio e H2O
- Ossa –> ossificazione nello sviluppo, mantenimento della desnità e attività di rimodellamento osseo favorendo la deposizione del calcio
- Sistema Nervoso centrale e periferico –> inibizione dell’apoptosi, modulazione stimolatoria (principalmente dopaminergica) e inibitoria (principalmente GABAergica) nel SNC, stimolatoria a livello dei motoneuroni
DHT: che cos’è e come funziona?
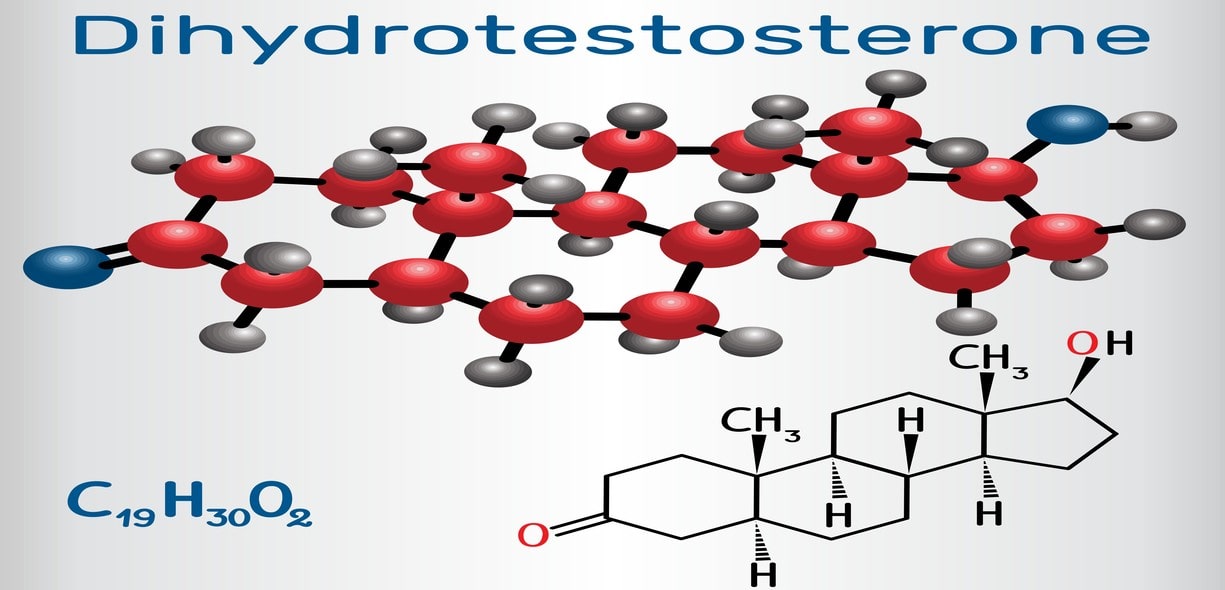
Il diidrotestosterone o DHT è la versione 5-alfa ridotta del Testosterone, cioè ha subito un processo enzimatico nel quale è saturato (ridotto) il doppio legame nel primo anello della molecola, rendendo questo ormone circa 5 volte più efficiente nel legame col recettore AR e rappresenta fino al 10% della conversione del testosterone. Questo aspetto ha fondamentale importanza nello sviluppo, infatti i tessuti che esprimono localmente alte quantità dell’enzima sono la cute, i genitali e il sistema nervoso e sono quei tessuti fortemente coinvolti nella pubertà.
I metaboliti del DHT, come gli isomeri dell’androstenediolo sembrano mediare gli effetti ansiolitici, “energizzanti”, pro-cognitivi e antidepressivi della somministrazione o sostituzione del testosterone, così come mediare parte degli effetti di diversi farmaci antidepressivi (SSRIs).
Per motivi poco chiari, forse interpretabili dal punto di vista evoluzionistico, il cuoio capelluto di molti uomini è molto sensibile al DHT: la comparsa e la progessione delle calvizie (alopecia androgenetica) è spesso mediata dal DHT, mentre negli altri distretti corporei ha l’effetto opposto cioè la crescita dei peli.
In medicina infatti sono usati farmaci (Finasteride) allo scopo di ritardare questo effetto negli uomini predisposti, che inibiscono l’enzima del cuoio capelluto riducendo quindi il segnale androgenico. Sono spesso accompagnati da spiacevoli effetti collaterali e disfunzioni sessuali, dovute alla carenza di DHT nel sistema nervoso.
Il DHT inoltre, purtroppo per noi, è inattivo sul muscolo scheletrico: la natura non ci vuole troppo muscolosi, infatti è presente in grandi quantità un enzima (3-Beta HSD) che inattiva il DHT convertendolo in metaboliti privi di rilevanti attività proteosintetica, come isomeri dell’androstenediolo.
Estradiolo: perché è importante anche nell’uomo?
Nell’uomo l’estradiolo è presente ed è necessario alla salute psicofisica, condivide numerosi ruoli analoghi agli ormoni femminili, quindi composizione corporea, equilibrio psichico, salute articolare e cardiovascolare. Deriva principalmente dall’aromatizzazione periferica degli androgeni, in particolare il testosterone ad opera di fegato, tessuto adiposo e tessuto muscolare.
Nell’uomo avere livelli troppo bassi di estradiolo è correlato ad astenia, osteoporosi, ipercolesterolemia e disfunzioni psicologiche e sessuali.
Anche valori troppo alti sono correlati a problematiche di vario tipo, come psicosi, disfunzione erettile, ipogonadismo, ritenzione di fluidi e sodio quindi ipertensione ed edema, ginecomastia (crescita della ghiandola mammaria) sovrappeso, obesità, diabete mellito di tipo 2 e sindrome metabolica.
A differenza del testosterone, l’estradiolo non sembra diminuire con l’avanzare dell’età, probabilmente per aumento della conversione periferica del testosterone.
Esami ormonali nell’uomo: come e perché variano i valori ormonali?
Nel sangue la maggior parte degli steroidi sono legati a proteine, nel caso degli androgeni le SHBG sono le proteine con maggior affinità di legame (60% del totale), mentre l’albumina lega in maniera più labile il testosterone (38% del totale). Le SHBG possono aumentare in caso di epatopatie, malnutrizione o elevate assunzioni di grassi, assuzione o elevati livelli di estrogeni o SERM e ormoni tiroidei; diminuiscono invece nel caso di assunzione o livelli elevati di androgeni, corticosteroidi, GH, obesità e diabete mellito di tipo 2, così come in una dieta ricca di glucidi (per stimolo insulinico).
La frazione libera (circa 2%) è quella che risulta “attiva” cioè in grado di essere convertita nei suoi metaboliti o di esplicare le funzioni di ormone tramite legame con proteine di membrana o recettori citosolici che verranno internalizzati nel nucleo cellulare.
| Ormone | Testosterone | T. Libero | DHT | Estradiolo | LH | FSH |
| Valori fisiologici | 260 – 1000 ng/dl | 50 – 210 pg/dl | 27 – 75 ng/dl | 15 – 50 pg/dl | 1.5 – 9.3 UI/L | 1.6 – 8.0 UI/L |
Gardner & Shoback, 2009 – Greenspan’s endocrinologia generale e clinica
L’alterazione più freuqente di questi valori nell’uomo è data da ipogonadismo che può essere (semplificando):
- primario –> cioè causa testicolare come ad esempio la sindrome di Klinefelter (cromosoma X in più) così come un danno al testicolo dovuto a traumi, interferenti endocrini o altre cause, insufficienza o insensibilità all’ LH delle cellule di Leydig, ripetuto abuso di AAS;
- secondario –> dovuto all’insufficienza di secrezione delle gonadotropine (LH e FSH) che può essere anche in questo caso genetica (sindrome di Kallman) o avere altre cause come l’obesità, traumi ipofisari o abuso di AAS.
L’ipogonadismo necessita di terapia sostitutiva, che spesso (ma a seconda del tipo può variare) è basata sul testosterone iniettabile (T. enantato o undecanoato i più usati), transdermico o più raramente in capsule oleose o pellets.
Altre terapie sono a base di gonadotropine umane come l’hCG (estratta dalle urine di donne gravide) o i SERM (come il clomifene o il tamoxifene) che antagonizzano il feedback negativo a livello dell’asse stimolando la secrezione di LH e FSH.
I metodi naturali per aumentare il testosterone, o meglio massimizzare la propria e individuale capacità endogena sono assolutamente low-cost, poco sensazionali ma affidabili al 100%.
Il più efficace è il dimagrimento! (sempre se necessario, ovviamente). Riducendo a livelli accettabili la massa adiposa, riduciamo l’eccessiva conversione di Testosterone in estradiolo, che come visto va a ridurre la secrezione di LH quindi riducendo a sua volta la produzione endogena di testosterone. Inoltre se come spesso purtroppo accade siamo insulinoresistenti o abbiamo il diabete di tipo 2, abbiamo una iperinsulinemia che riduce le SHBG liberando più testosterone…
Qualcuno giustamente si chiederà: ma non è il testosterone libero quello attivo?
Certamente, ma il problema è che se il nostro testosterone liberato dalle SHBG viene convertito in estradiolo (perchè abbiamo troppo grasso), non abbiamo nessun beneficio dato dalla sua quota libera.
Recuperando la sensibilità insulinica inoltre si fa un grosso favore al testicolo e al sistema cardiovascolare, che ritorna a produrre fisiologicamente la giusta quantità di ossido nitrico (NO) un potente vasodilatatore endogeno e si riduce la formazione di radicali liberi (ROS) e prodotti di glicazione avanzate (AGE), tutto a beneficio della salute psicofisica.
Anche il problema opposto esiste, infatti come visto nell’articolo sulla leptina, una carenza di tessuto adiposo è dannosa anche nell’uomo, la leptina infatti segnala all’ipotalamo che è presente una adeguata riserva energetica e che quindi si possono mantere anche i processi non vitali, quali la riproduzione.
Rimanere tirati al 5% tutto l’anno non fa bene nè piscologicamente nè fisicamente.
Ormoni maschili in pillole
Il testosterone è poco biodisponibile per ingestione anche se esistono dei preparati per l’assunzione orale. Sono poco pratici, vanno assunti con pasti ricchi in lipidi più volte al giorno per arrivare a livelli fisiologici di testosterone.
Diverso è il caso di AAS in passato testati per la terpia sostitutiva come il metiltestosterone e il fluossimesterone, androgeni sintetici piuttosto tossici per il fegato, che hanno un limitato effetto di primo passaggio epatico grazie ad una modifica chimica cioè un legame 17-alfa metilico che modifica letteralmente la “forma” della molecola, rendendola difficile da metabolizzare dal fegato. Inoltre sono piuttosto deleteri sui livelli di coelsterolo, arrivando fino a dimezzare il colesterolo “buono” HDL e aumentando quello “cattivo” LDL.
In tempi recenti si sta sperimentando la “pillola maschile” ovvero un anticoncezionale orale per l’uomo.
Questo nasce dalla variabile affidabilità dell’uso del solo testosterone, anche a dosi sovrafisiologiche, nell’indurre azoospermia nell’uomo. Complicato inoltre dal periodo medio di 3 mesi per completare la spermatogenesi, cioè il processo deve essere bloccato per almeno 3 mesi di fila per essere efficace a differenza della donna, e non vi è garanzia di tempo entro il quale si abbia questa soppressione della fertilità.
Rimangono numerosi dubbi e necessità di sperimentazioni su questa nuova pillola, in quanto non è fisiologico sopprimere il testosterone e rimpiazzarlo con un ormone piuttosto differente (il dimetandrolone, DMAU, cugino del famoso nandrolone) che non aromatizza (carenza di estrogeni), non si alfa riduce (possibile carenza a livello del sistema nervoso) e che ha forte attività progestinica (assente nel Testosterone e DHT).
Dai trial risulta inoltre che causa aumento di peso (non specificato se grasso o magro), riduzione del colesterolo HDL, disfunzioni sessuali, reversibilità a lungo termine sulla feritilità ancora non così chiara, vista la diversa fisiologia maschile.
Conclusioni sugli ormoni maschili (o androgeni)
Concludendo, gli ormoni “maschili” anche definiti come androgeni, sono responsabili delle differenze piscofisiche tra i sessi biologici e fondamentali nella salute psicofisica. Il testosterone è responsabile soprattutto della maggior muscolarità rispetto alla donna, mentre gli effetti tipicamente androgeni sono mediati dalla conversione in DHT. L’estradiolo per quanto spesso associato al mondo femminile è fondamentale nella salute anche dell’uomo da un punto di vista di fisico che psicologico, anche se chiaramente in rapporti quantitativamente diversi.
Riassumendo in punti quanto visto:
- Il Testosterone è il principale androgeno nell’uomo
- La sua sintesi è regolata dall’asse endocrino ipotalamo-ipofisi-testicolo ed è strettamente regolato
- Gli effetti androgeni sono in realtà in gran parte mediati dal DHT
- L’estradiolo è ugualmente importante nella salute psicofisica dell’uomo
- Esistono dei range fisiologici di tali ormoni, e come per altri ormoni l’equilibrio è la chiave di tutto
- Quantità sovrafisiologiche sono pericolose in modo dose-dipendente
- In futuro probabilmente saranno disponibili pillole anticoncezionali al maschile, che tuttavia sono ancora in fase di sperimentazione
- Per aumentare il testosterone senza farmaci bisogna avere un livello di grasso corporeo accettabile e non estremo, alimentarsi adeguatamente senza estremismi sui macronutrienti
- Il colesterolo alimentare non aumenta il testosterone, tantomeno il colesterolo LDL endogeno
Bibliografia sugli ormoni maschili
- William Lewellyn, 2011 – Anabolics 11th edition
- Gardner & Shoback, 2009 – Greenspan’s endocrinologia generale e clinica
- Low Testosterone Associated With Obesity and the Metabolic Syndrome Contributes to Sexual Dysfunction and Cardiovascular Disease Risk in Men With Type 2 DiabetesChristina Wang, Graham Jackson, T. Hugh Jones, Alvin M. Matsumoto, Ajay Nehra,Michael A. Perelman, Ronald S. Swerdloff, Abdul Traish, Michael Zitzmann, GlennCunningham Diabetes Care Jul 2011, 34 (7) 1669-1675;
- Wibowo, Erik & Schellhammer, Paul & Wassersug, Richard. (2010). Role of Estrogen in Normal Male Function: Clinical Implications for Patients With Prostate Cancer on Androgen Deprivation Therapy. The Journal of urology. 185. 17-23. 10.1016/j.juro.2010.08.094.
- Arthi Thirumalai, Jonas Ceponis, John K Amory, Ronald Swerdloff, Vijaya Surampudi, Peter Y Liu, William J Bremner, Eric Harvey, Diana L Blithe, Min S Lee, Laura Hull, Christina Wang, Stephanie T Page, Effects of 28 Days of Oral Dimethandrolone Undecanoate in Healthy Men: A Prototype Male Pill, The Journal of Clinical Endocrinology & Metabolism, Volume 104, Issue 2, February 2019, Pages 423–432,
- Gava, G., & Meriggiola, M. C. (2019). Update on male hormonal contraception. Therapeutic advances in endocrinology and metabolism, 10, 2042018819834846. doi:10.1177/2042018819834846
- Swee, D. S., & Gan, E. H. (2019). Late-Onset Hypogonadism as Primary Testicular Failure. Frontiers in endocrinology, 10, 372. doi:10.3389/fendo.2019.00372
- Walther A, Breidenstein J, Miller R. Association of Testosterone Treatment With Alleviation of Depressive Symptoms in Men: A Systematic Review and Meta-analysis. JAMA Psychiatry.2019;76(1):31–40. doi:10.1001/jamapsychiatry.2018.2734
- Bhasin, S., & Basaria, S. (2011). Diagnosis and treatment of hypogonadism in men. Best Practice and Research: Clinical Endocrinology and Metabolism. https://doi.org/10.1016/j.beem.2010.12.002

















